ปฏิกิริยาเคมีในเซลล์ของสิ่งมีชีวิต
แบบฝึกหัด
EASY
ปฏิกิริยาเคมีในเซลล์ของสิ่งมีชีวิต
เนื้อหา
ปฏิกิริยาเคมีในเซลล์
ของสิ่งมีชีวิต
อะตอมของธาตุมารวมกันเป็นสารประกอบโดยการสร้างพันธะซึ่งอยู่ในรูปพลังงานพันธะ ปฏิกิริยาเคมีแบ่งได้เป็น 2 ประเภท คือ
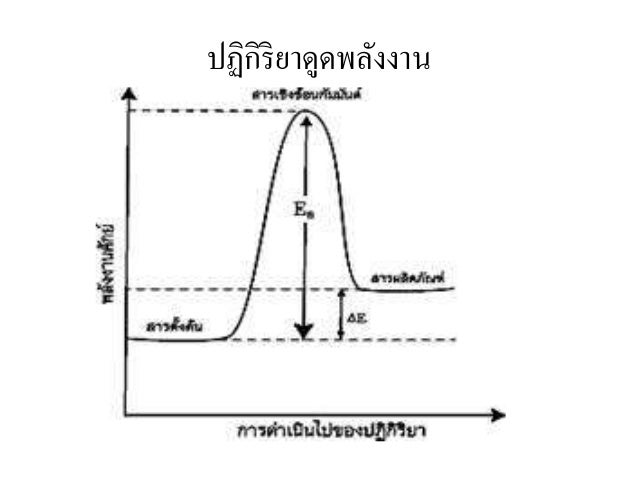
Endergonic reaction
Exergonic reaction
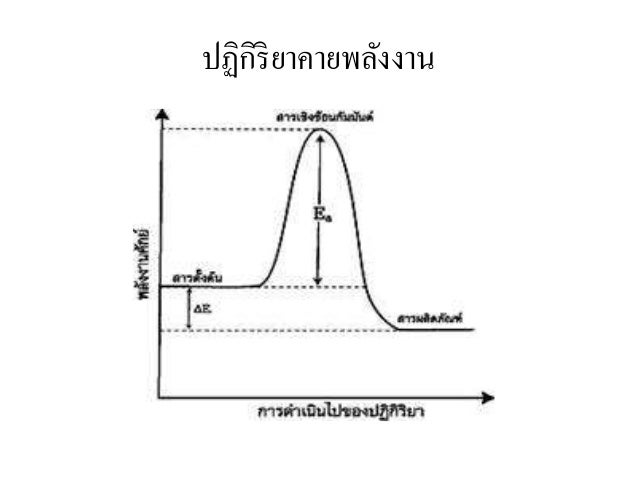
สิ่งแวดล้อมเพื่อให้ปฏิกิริยาสิ้นสุดด้วยสารผลิตภัณฑ์
ที่มีพลังงานพันธะต่ำกว่าสารตั้งต้น
เป็นตัวเร่ง
คุณสมบัติของเอนไซม์ได้แก่
- Specificity มีความจำเพาะ โดยมี active site หรือบริเวณเร่ง ที่สามารถจับกับสารตั้งต้นได้อย่างจำเพาะ
- Globular proteins เอนไซม์ส่วนมากเป็นโพลีเปปไทด์เรียงตัวกันทำให้เกิดรูปร่างและโครงสร้างเฉพาะ
- Sensitive รูปร่างเฉพาะนี้ อาจถูกเปลี่ยนแปลงได้โดยอุณหภูมิ สภาวะ กรดเบสที่เหมาะสม
- Reusable เมื่อเอนไซม์เร่งปฏิกิริยาแล้ว ถ้าปัจจัยอุณหภูมิและภาวะกรดเบสคงที่ เอนไซม์อยู่ในโครงสร้างและรูปร่างเดิม สามารถกลับมาเร่งปฏิกิริยาได้อีก
ปัจจัยที่มีผลต่อการทำงานของเอนไซม์ได้แก่
- ความเป็นกรดเบส เพราะมีผลต่อขั้วของโปรตีน ตลอดไปจนถึงรูปร่างของโปรตีน
- อุณหภูมิในช่วง 25 ถึง 40 องศา เพราะมีผลต่อการสร้างหรือแตกพลังงานพันธะของโปรตีน
- ความเข้มข้นของเอนไซม์และสารตั้งต้น ทำให้อัตราการเร่งปฏิกิริยาช้าหรือเร็ว เนื่องจาก อัตราส่วนจำนวนสารตั้งต้นต่อเอนไซม์ มีผลต่ออัตราการ reusable
ของเอนไซม์ - โคแฟกเตอร์ สารอื่นๆ ที่ทำหน้าที่ช่วยเอนไซม์ 1) เป็นสารอินทรีย์ขนาดเล็กเรียกว่า co-enzyme เช่น วิตามินต่างๆ 2) ส่วนที่ไม่ใช้เอนไซม์ โดยมากเป็นธาตุและ สารโลหะ เช่น Zn2+, Mg2+, Fe2+, Na+ เป็นต้น
- ตัวยับยั้งเอนไซม์ enzyme inhibitor มีผลต่อการทำงานของเอนไซม์ เนื่องจากตัวยับยั้งเอนไซม์มีลักษณะจำเพาะคล้ายคลึงกับเอนไซม์ ซึ่งสามารถจับกับสารตั้งต้น จึงเป็นตัวขัดขวางการทำงานของเอนไซม์ ตัวยับยั้งเอนไซม์แบบชั่วคราว reversible inhibitors
เป็นการยับยั้งแบบไม่แข็งแรง ส่วนอีกประเภท คือตัวยับยั้งเอนไซม์แบบถาวร irreversible inhibitors
เกิดการจับกับเอนไซม์แบบเสถียร ทำให้ไม่สามารถเร่งปฏิกิริยาอีกได้ เช่น nerve gas ถ้าได้รับเข้าสู่ร่างกาย ในปริมาณมาก อาจทำให้เสียชีวิตได้ เพราะขัดขวาง
เมตาบอลิซึมต่างๆในร่างกาย
ทฤษฎีที่ว่าด้วยการทำงานอย่างเฉพาะเจาะจงของเอนไซม์
- Induced fit theory ทฤษฎีการใส่ถุงมือ
ว่าสารตั้งต้นเหนี่ยวนำให้เอนไซม์ปรับรูปร่างจับกับ
สารตั้งต้นได้อย่างเหมาะสมเปรียบเช่นการใส่ถุงมือ - Lock and key theory ทฤษฎีแม่กุญแจและลูกกุญแจ ว่าสารตั้งต้นและเอนไซม์มีรูปร่างเฉพาะที่พอดีกันเปรียบเหมือนแม่กุญแจและลูกกุญแจ โดยที่โครงสร้างไม่เปลี่ยนแปลง
ตัวอย่างประเภทของเอนไซม์
Synthetase (ligase) เป็นเอนไซม์ที่เกี่ยวกับการสังเคราะห์หรือเชื่อมโมเลกุลในสาย DNA
Transferase เป็นเอนไซม์ที่เกี่ยวข้องกับ
การเปลี่ยนหมู่ฟังก์ชัน
Hexokinase เป็นเอนไซม์ทีเร่งปฏิกิริยาการแยกหมู่ฟอสเฟตออกจากน้ำตาล C6
Isomerase เป็นเอนไซม์ที่เกี่ยวกับการเปลี่ยนไอโซเมอร์